最近几年,非小细胞肺癌(NSCLC)的诊疗已经有了显著改变,一旦确定患有该病,则必须根据组织学及突变信息进行进一步分类。对于靶向研究方面的进展,已经可以通过受体的单克隆抗体(mAb)或小分子酪氨酸激酶抑制剂(TKI)对相关突变进行抑制。
虽然根据经验来说,含铂的二联化疗仍是无基因突变的进展期 NSCLC 治疗金标准,但靶向治疗已经显著改善了患者的预后及生活质量。近期,澳大利亚的 Chan 及 Hughes 两位教授在近期的 Translational Lung Cancer Research 发表文章,就 NSCLC 靶向治疗相关问题进行了综述,现为大家介绍如下。
NSCLC 不是一个独立的病变,而实际是多种我们正在阐明和了解的、具有独特分子标记的病理状态。广义说来,主要亚型有肺腺癌、鳞状细胞癌及大细胞癌。这种分类仅适用于无驱动突变的进展期 NSCLC 细胞毒性药物化疗选择,如腺癌中培美曲塞效果好,组织学类型为鳞癌的患者要考虑贝伐单抗的不良反应。
但目前对 NSCLC 的合理治疗,需对肿瘤进行预测性及预后性标志物的筛查,以帮助预测靶向治疗敏感性、并估测预后。对于 NSCLC 来说,最近这些年的大部分工作在于表皮生长因子受体(EGFR)酪氨酸激酶抑制剂及克唑替尼分别成功的抑制了 EGFR 的突变及间变性淋巴瘤激酶(ALK)的异常融合。
靶向药物目前已经进行合理设计,以抑制导致序贯性临床表现的特定突变。本文就是对 NSCLC 中已确定的驱动突变主要类型、相关靶向治疗进行综述,并对未来进行展望。
NSCLC 中的信号通路靶点
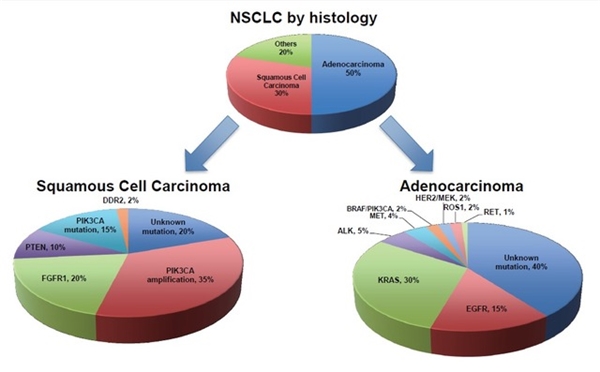
NSCLC 的组织学分类中,不管是传统分法、还是现在简化的分法,都包括腺癌、鳞状细胞癌及大细胞癌。高达 60% 的腺癌、50-80% 的鳞癌中具有已知的肿瘤性驱动突变(图 1)。这类受体或蛋白激酶的突变可导致涉及多条信号通路的复杂级联反应(图 2)。最终,导致不受调控的生长、增生及存活。
图 1. NSCLC 组织学分类及相关突变(见下图)
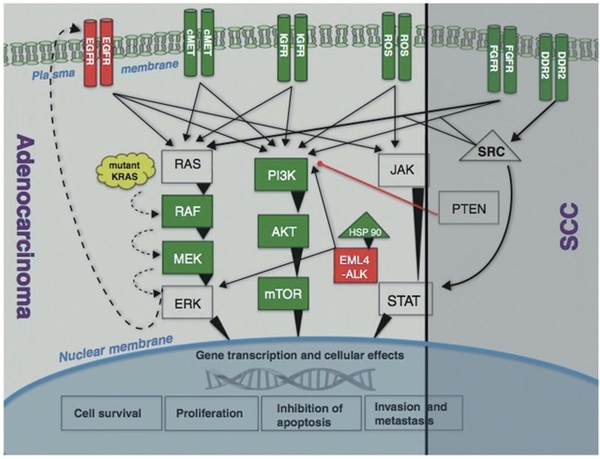
图 2. NSCLC 中分子通路及潜在靶点概述(见下图)
成功靶向治疗包括对上调通路的识别、以及通过小分子抑制剂或受体单克隆抗体对其进行抑制。NSCLC 中研究最深入的就是 EGFR 及其下游通路间的相互作用。
表皮生长因子受体
表皮生长因子受体(EGFR、或 ErbB1、HER1)属于受体酪氨酸激酶家族,可触发一系列信号通路,导致细胞生长、增殖及存活。这类通路包括 RAS-RAF-MEK-ERK 或 MAPK 通路及 PI3K-AKT-mTOR 通路。
导致 EGFR 激活的主要机制有三种:恶性细胞中 EGFR 表达增加、恶性细胞导致配体增强、恶性细胞中 EGFR 活性突变。高达 40-80% 的 NSCLC 中 EGFR 过表达,因此是一个大有潜力的转化治疗靶点。不过,后来发现 EGFR 较好的治疗靶点是其活性突变、而不是过表达。
两个最常见的突变是 19 号外显子缺失(60%)及位点 858 处亮氨酸被精氨酸取代产生的 L858R 错义替换(35%),导致受体失去配体结合从而构成性活化。突变的 EGFR 可被小分子酪氨酸激酶(如吉非替尼及厄洛替尼)或小分子抗体(如西妥昔单抗)来抑制。
吉非替尼和厄洛替尼均为第一代 EGFR 酪氨酸激酶抑制剂,二者均为 EGFR 中酪氨酸激酶结构域 ATP 的可逆性竞争抑制剂,从而导致下游通路的阻断。早期对未经选择的患者进行 EGFR 酪氨酸激酶抑制剂试验,那时还不知道现在已知的这些临床及分子预测标记。
试验完成后,亚组分析发现与效果有关的特征有组织学为腺癌、亚洲裔人群、无吸烟史。对酪氨酸激酶抑制剂有效患者的组织学标本进行分子检测,发现 EGFR 的体细胞活性突变支持该药有效。
EGFR 突变的比例在不同种族各异,亚洲人群高达 50% 的腺癌具有 EGFR 的活性突变,而白种人则仅为 10-15%。不过,目前还没有可靠的临床表现或特征可以准确预测 EGFR 突变,因此所有肿瘤均应进行突变检查。
1. EGFR 突变的 NSCLC
过去十年里,NSCLC 治疗方案中最显著的改变可能就是 EGFR 酪氨酸激酶抑制剂用于具有 EGFR 靶向性驱动突变患者一线治疗了。
这方面的标志性研究就是易瑞沙泛亚洲研究(IPASS)了,该研究对东亚国家 1217 例未曾治疗过的 IIIB 或 IV 期腺癌随机分为吉非替尼或卡铂加紫杉醇化疗组。结果发现 12 个月时的无进展生存(PFS)在吉非替尼组要显著优于化疗组。EGFR 活性突变患者应用吉非替尼时的无进展生存更要显著长于应用化疗者。相反,EGFR 野生型患者对化疗的反应性更好。
First-SIGNAL 研究也在不吸烟的腺癌患者中验证了上述结论:该研究对一线应用化疗及吉非替尼进行了比较,总的无进展生存未见显著差异,但在回顾吉非替尼组患者时发现,EGFR 活性突变确实可以预测总有效率(ORR)更好、无进展生存显著延长。
后来还有研究对 EGFR 突变 NSCLC 患者、而不像较早研究那样仅从大量临床指标来选择患者进行了吉非替尼、厄洛替尼或阿法替尼与化疗间的比较,发现一线 EGFR 酪氨酸激酶抑制剂治疗患者的总有效率、无进展生存及生活质量均比化疗者要好。
因此,前述的预测性生物学标记现在已经成为标准,并且如果 EGFR 具有活性突变则应将 EGFR 酪氨酸激酶抑制剂用作一线治疗。不过,对易瑞沙泛亚洲研究的长期随访表明,EGFR 酪氨酸激酶抑制剂用于一线治疗无总生存获益的原因很可能是由于进展后的广泛影响所致。
目前,尚未发表直接比较一线 EGFR 酪氨酸激酶抑制剂效果的头对头试验(即非安慰剂对照试验)。一般说来,这类制剂的效果类似,因此选择药物时需根据不良作用、用药时的临床表现而定。已有研究直接比较了阿法替尼与吉非替尼用于 EGFR 突变腺癌一线治疗(临床试验编号 NCT01466660)。
EGFR 酪氨酸激酶抑制剂辅助用于可切除的 I 至 III 期 NSCLC 仍未确定。术后做或不做化疗时辅助应用厄洛替尼、尤其是用于 EGFR 突变者的研究,仍在进行中,2016 年有望完成研究(临床试验编号 NCT00373425)。由于此前的研究对于未经筛选的患者辅助应用吉非替尼证实无效,因此该研究的数据尤其令人感兴趣。
2. EGFR 野生型及 EGFR 状态未知的进展期 NSCLC
大部分肿瘤无 EGFR 活性突变(称之为野生型),因此这类人群中酪氨酸激酶抑制剂的作用有争议。就一线治疗来说,根据 IPASS 及 TORCH 研究结果,相关指南均禁止一线应用酪氨酸激酶抑制剂。
对于二线治疗来说,TAILOR 试验比较了厄洛替尼和多西紫杉醇在 EGFR 野生型肿瘤中的应用。所有的研究目标如总有效率、无进展生存、总生存(OS)方面,多西紫杉醇组均优于厄洛替尼组。这支持仍将细胞毒性化疗药物作为无靶向驱动突变 NSCLC 患者的首选治疗方案。
EGFR 酪氨酸激酶抑制剂加入标准的含铂二联化疗方案,是否可改善预后?关于该问题有四项研究。INTACT1 及 INTACT2 关注的是吉非替尼,而 TRIBUTE 和 TALENT 关注的是厄洛替尼。四项研究均证实无效、对生存无影响。
经含铂二联化疗后出现进展的患者,预后仍很差。多西紫杉醇及培美曲塞均证实为二线有效药物,但仍需更多治疗方案、尤其是对那些无法进一步化疗者。INTEREST 研究是一项在未经选择的二线患者中比较吉非替尼与多西紫杉醇的多国 III 期随机试验。在总生存方面,吉非替尼并未表现出优越性。
进一步研究表明,吉非替尼和厄洛替尼用于二线治疗时,与化疗相比在有效率、无进展生存和生活质量方面要更好,但总生存方面无显著差异。
EGFR 状态未知、且不适合化疗的患者,III 期研究 TOPICAL 发现一线应用厄洛替尼相比安慰剂来说要有显著生存获益,但仅限于那些 28 天内出现皮疹者。还要注意的是,未能出现厄洛替尼相关皮疹的患者,在生存方面要次于安慰剂组。
还有两项 III 期研究比较了 EGFR 酪氨酸激酶抑制剂和安慰剂用于未选择患者二线及三线治疗时的情况。第一项是 BR.21 试验,也是迄今为止唯一一项证实 EGFR 酪氨酸激酶抑制剂具有总生存获益的试验;ISEL 试验中吉非替尼未见显著生存获益。
新型 EGFR 酪氨酸激酶抑制剂埃可替尼(icotinib)在此前治疗过、未经选择的进展期 NSCLC 患者头对头试验中也未见比吉非替尼更有优越性。因此,对于无更好化疗方案的 EGFR 状态未知或野生型者,厄洛替尼在铂类为主化疗后作为二线或三线治疗可能有益。
初始诱导化疗后转为 EGFR 酪氨酸激酶抑制剂维持治疗,已经表现出少许、但却为实质性生存获益。用吉非替尼的 WJTOG0203 和 INFORM 试验及用厄洛替尼的 SATURN 和 IFCT-GFPC0502 试验具有类似获益。SWOG S0023 试验则明确表明放化疗后吉非替尼未见获益。实际由于安慰剂似乎具有更好的无进展生存和总生存,因此,吉非替尼似乎还有不良反应。
3. 抗 EGFR 的单克隆抗体
单克隆抗体是抑制 EGFR 活性和信号的另一方案。除竞争性抑制胞外结构域的配体结合外,还可形成被内吞及降解的抗体 - 受体复合物。目前可用的抗 EGFR 单克隆抗体包括西妥昔单抗、necitumumab、帕尼单抗、马妥珠单抗。
两项 III 期试验 FLEX 及 BMS009 在进展期 NSCLC 患者中研究了西妥昔单抗与含铂二联化疗联用的效果。FLEX 试验表明总生存的中位数略有改善,而较小的 BMS099 试验则为阴性结果。
还有两项 III 期试验正在研究 necitumumab。非鳞的 NSCLC 中正在进行的 INSPIRE 试验、非小细胞鳞癌中已经完成的 SQUIRE 试验对顺铂 - 吉西他滨加 necitumumab 进行了研究。SQUIRE 试验报道总生存有改善。其他正在进行 II 期试验的单克隆抗体还有帕尼单抗及马妥珠单抗。
4. EGFR 靶向性治疗的耐药性
尽管 EGFR 酪氨酸激酶抑制剂已经引起了 EGFR 突变型 NSCLC 治疗的变革,但对于 7-12 个月后出现进展的患者则大部分疗效均未证实可以持续。耐药性可以原本就有、也可以是应用靶向性药物后出现的,可表现为同一肿瘤内的耐药克隆、也可是同一患者体内的不同肿瘤。
大部分患者均会出现「获得性耐药」,可能是 EGFR 二次突变、也可能是 EGFR 非依赖性通路的活化。因此,临床医生应考虑对出现进展的肿瘤重新活检、以评估该肿瘤的生物学行为。
EGFR 耐药机制中最常见的(约 50%)是同时出现 20 号外显子突变,编码 T790M。苏氨酸被蛋氨酸取代,改变了激酶结构域的构象并增强了其对 ATP 的亲和力,因此就对第一代可逆性酪氨酸激酶抑制剂的亲和力降低了。
第二种常见的机制(约占 5-10%)是 MET 扩增、通过 PI3K-Akt-mTOR 信号通路而绕过了 EGFR 的抑制。其他耐药机制还有 PIK3CA、HER2、BRAF、STAT3、AXL 激酶的突变及 CRKL 的扩增,还有 5% 出乎意料的转化为了小细胞肺癌。
尽管我们对获得性耐药机制的理解已经取得了显著进展,但高达 30% 的耐药机制还是未知的,因此经验性细胞毒性药物化疗仍是治疗方案。
与化疗不同,一旦确定异常通路,则可合理的解释靶向性治疗的耐药。二代不可逆性 ErbB 家族酪氨酸激酶抑制剂如阿法替尼,可共价结合 EGFR/HER1 及 HER2,从而克服 T790M 突变。
EGFR 酪氨酸激酶加西妥昔单抗双重阻断 EGFR 在小鼠模型中成功之后,目前已经在进一步试验。MET 及 T790M 的双重抑制在小鼠模型中也表现出了前景不错的效果,目前正在人类进行 MET/ALK 抑制剂(克唑替尼)加全 HER 抑制剂(dacomitinib)的临床试验。
第三代 EGFR 酪氨酸激酶抑制剂如特异性针对 T790M 的 CO-1868 及 AP26113,在获得性耐药中已经表现出了有效的初步证据、且不良反应也可以接受。尽管靶向治疗具有耐药性,但如果联合治疗相比一线单药来说更加有效、且综合考虑不良反应和费用等,那么未来或许应该是选择合理的联合治疗
EML4-ALK 阳性 NSCLC
ALK 基因最初是 1994 年在非霍奇金淋巴瘤中发现的,是由于染色体异位导致 ALK 与核仁磷酸蛋白(NPM)融合所致。2007 年,Soda 等对非小细胞肺癌进行研究时发现了相同的 ALK 基因,但此时却是因为染色体 2p 内小的倒位导致 ALK 和棘皮动物微管相关蛋白样蛋白 4(EML4)融合。
EML4-ALK 融合型癌基因存在于高达 3-7% 的 NSCLC,可促进恶性生长及增殖。相比 EGFR 来说,ALK 重排更可能见于特殊人群:吸烟少或不吸烟的年轻腺癌患者、组织学上多为印戒细胞者。
具有 ALK 重排的肿瘤,自然不会有 EGFR 或 KRAS 突变,且意味着是一种「癌基因依赖性」表型,即单一基因产物可导致恶性改变。
与 EGFR 不同,ALK 用于治疗靶点的过程更加合理;从发现、肿瘤前瞻性分型及有针对性的设计试验,到测试其抑制剂及患者取得阳性结果均如此。
克唑替尼是一种抑制 ALK、MET 及 ROS 酪氨酸激酶的口服小分子抑制剂,2011 年仅完成 I/II 期试验,发现在此前未治疗过的患者中有效率极佳,FDA 就批准了其上市。最终结果证实,无进展生存为 9.7 个月;总生存中位数的数据还没公布,但 ALK 阳性 NSCLC 患者回顾性分析的数据表明,应用克唑替尼具有相关的生存获益。
值得注意的是,ALK 阳性本身并非有利的预后因素,因为不治疗的患者预后和普通的 NSCLC 患者预后一样差。
已经证实克唑替尼用于此前曾接受过含铂二联化疗患者时,要比二线化疗有优越性。克唑替尼治疗者的无进展生存为 7.7 个月,而培美曲塞或多西紫杉醇化疗者为 3.0 个月。总生存无差异,可能是由于具有大量干扰因素、且对生存的随访不足所致。
克唑替尼的不良作用相对轻,主要是轻度视觉障碍(闪光感、视物模糊)及胃肠道副作用。16% 的患者可见肝脏转氨酶升高较显著,一例发展为致死性肝功能衰竭。间质性肺病可见于 2% 的患者,2 例死亡。总体而言,克唑替尼治疗的患者症状减轻及生活质量改善要更好一些。
III 期试验 PROFILE1014 正在对克唑替尼用作未经治疗患者的一线治疗和铂类 - 培美曲塞化疗进行比较,目前已经完成了患者入组。近期有望出结果,如果结果阳性,则会夯实克唑替尼用作 ALK 阳性 NSCLC 患者治疗金标准这一主张。
如 EGFR 酪氨酸激酶抑制剂一样,ALK 重排 NSCLC 患者应用克唑替尼也会出现耐药性。这方面已经发现了有多种机制,如 ALK 扩增,EGFR/HER2、HER2 和 HER3 的上调,cKIT 扩增,包括 L1196M 在内(如同 EGFR 中的 T790M)的多种 ALK 突变。
对于克唑替尼耐药的患者,已经有一项 I 期试验表明,二代 ALK 抑制剂色瑞替尼(LDK378)的总有效率为 56%。相比克唑替尼来说,其对 ALK 的抑制作用高达 20 倍,且有望克服 L1196M 突变。尤其受鼓舞的是,用于具有多种已知耐药机制、以及无明确突变的患者时,其有效率也近似。
其他类似的二代 ALK 抑制剂如 alectinib,正在研究中;但如 EGFR 时一样,未来有望找到一种克服 ALK 耐药的合理方案。
NSCLC 中的 K-RAS 突变
K-RAS(Kirsten 大鼠肉瘤 2 病毒致癌基因家族)属于 GTP 酶家族成员,可经多种酪氨酸激酶(如 EGFR 及 MET)转换生长信号(图 2)。KRAS 活性突变导致构成性信号通路传导,存在于约 30% 的腺癌及 4% 的鳞癌。KRAS 突变更多见于白人、此前或现在吸烟者,且与 EGFR 或 ALK 突变互不共存,且与预后较差、对 EGFR 酪氨酸激酶抑制剂化疗耐药有关。
尽管 KRAS 是 NSCLC 中最早了解的致癌性驱动基因,但有效的靶点仍是治疗中的挑战。用 salirasib 直接发挥 RAS 抑制作用没能成功,因此目前在尝试新的方案以抑制 RAS/RAF/MEK/ERK 及 PI3K/AKT/mTOR 通路中的下游分子。其他还有针对 KRAS 突变细胞中升高的热休克蛋白(HSP90)的方案。
最近,针对进展期 KRAS 突变 NSCLC 患者进行的 II 期试验中,MEK1/MEK2 抑制剂司美替尼与多西紫杉醇合用时具有无进展生存获益。目前正在与 AKT 抑制剂联合进行临床前试验的基础上进行验证性 III 期试验,试验名称为 SELECT-1。
NSCLC 中的 MET 扩增
间质上皮转化(MET)因子的扩增可见于约 5% 的肺腺癌,并导致其基因产物 - 肝细胞生长因子受体(HGFR)的过表达,该受体参与了细胞增殖、迁徙、浸润及转移。抑制 MET/HGFR 介导细胞生长有多种策略,如 HGF 拮抗剂、抗 HGFR 单克隆抗体、抗 MET 单克隆抗体、MET 酪氨酸激酶抑制剂如 tivantinib、cabozantinib,当然还有克唑替尼。
MET 及 EGFR 对于细胞的生长似乎具有协同作用,且 MET 扩增也是 EGFR 酪氨酸激酶抑制剂获得性耐药的第二常见原因。在此考虑下,分别用厄洛替尼及 tivantinib 双重抑制 EGFR 及 MET,II 期试验数据表明对于 KRAS 突变者具有无进展获益,因此全球性 III 期试验 MARQUEE 在非鳞的非小细胞肺癌中进行了测试。
II 期试验中,针对 MET 的单克隆抗体 onartuzumab 也表现出了有潜力的结果,因此在 MetLung 试验中对于 MET 阳性 NSCLC 结合厄洛替尼进行了 III 期试验。
尽管上述早期试验的结果令人满意,但用 MET 酪氨酸激酶及 MET 单克隆抗体的验证性试验仍得出了让人失望的结果,已经有两项 III 期研究提前终止了。MARQUEE 在 2012 年年末终止了,原因是中期分析发现对总生存这个主要指标无效。MetLung 也因为无效而提前终止了。
有趣的是,2013 年欧洲肿瘤大会上展示了 MARQUEE 亚组分析的结果,表明 MET 免疫组化强阳性的肿瘤中具有无进展生存和总生存获益。未来针对 MET 抑制,似乎需要更加明确的预测性生物标记,以加强对患者的筛选。
NSCLC 中的 ROS1 重排
ROS1 重排是 2007 年才发现的,约 1-2% 的非小细胞肺癌患者具有不同的 ROS1 融合亚型。尽管其在人类组织中的功能还未知,但在正常肺组织中表达最高。与其他受体酪氨酸激酶一样,ROS1 作用于多个下游通路,如 RAS/RAF/MEK 或 MAPK、JAK/STAT3、PI3K/AKT/mTOR 通路(图 2)。
ROS 两种重排具有相同的临床表型:年轻患者、不吸烟的腺癌患者。ROS1 和 ALK 间具有约 50% 的序列同源性,因此 ALK 抑制剂如克唑替尼可能的确对两种激酶均有抑制。实际上,克唑替尼在 I 期试验中已经表现出了部分活性,但同时,获得性耐药似乎限制了激酶抑制剂的长期效果。特异性 ROS1 抑制剂如 foretinib,目前正在研究中。
NSCLC 中的 RET 融合
RET 是一种新型融合基因,涉及驱动蛋白家族成员 5B(KIF5B)及其他如 CCDC6、NCOA4、TRIM33。可见于约 1-2% 的肺腺癌,且主要为非吸烟者。目前尚无特异性 RET 抑制剂可用,但多重激酶抑制剂如凡德他尼(II 期)及克唑替尼(III 期)正在 RET 融合阳性 NSCLC 中进行研究。
NSCLC 中的 HER2 过表达及突变
人表皮生长因子 2(HER2/ErbB2/neu)如 EGFR/HER1 是酪氨酸激酶受体中 ErbB 家族成员之一,可通过与其他 ErbB 受体同源或异源性二聚化而活化。
HER2 过表达可见于高达 20% 的 NSCLC,但 HER2 突变率不高,最多 3-4%。NSCLC 中对其进行阻断的基本原理是借鉴了 HER2 阳性乳腺癌中的成功应用,不过,曲妥珠单抗联合化疗用于 NSCLC 的 II 期试验,迄今为止仍是阴性结果。
NSCLC 中的 BRAF 突变
NSCLC 中 BRAF 突变不常见,占所有病例的 5% 以下。作为 RAS/RAF/MEK/ERK 或 MAPK 通路的重要部分,BRAF 抑制似乎也是合理的,尤其是酪氨酸激酶抑制剂已经可以用于恶性黑色素瘤的情况下。
不过,对于具有 V600E 特异突变者,仅约半数治疗有效。目前,一项 II 期试验正在研究 BRAF 及 MEK 抑制剂即达拉非尼和曲美替尼联合应用于 IV 期 NSCLC。
鳞状细胞癌
尽管有那么多的通路及靶向药物,但大多是用于腺癌。鳞状细胞癌的靶向治疗还在研究阶段。最近,自癌症基因组图谱中得出的关于鳞状细胞癌分子病理学相关发现已经确定了几个重要信号通路。尽管这些通路可以被抑制,但还缺乏临床意义上的获益。进一步研究,有望在不久的将来看到鳞状细胞癌靶向制剂成为现实。
磷脂酰肌醇 3 激酶(PIK3CA)通路是具有 PIK3CA 突变及扩增、以及 PTEN 肿瘤抑制基因丢失的鳞状细胞癌中最常见的改变之一。NSCLC 患者中正在进行 PI3K 抑制剂 buparlisib 联合化疗的 II 期试验。
成纤维细胞生长因子受体 1(FGFR1)是另一条可开发的通路,其过表达可见于高达 20% 的鳞状细胞癌,而腺癌中仅 3%。FGFR 抑制剂如布立尼布(brivanib)及其他多重激酶抑制剂均在体内试验中展现出了阳性结果,目前正在进行早期试验。
盘状结构域受体 2(DDR2)是一种酪氨酸激酶受体,可见于高达 4% 的鳞状细胞癌。DDR2 的配体是胶原,参与了细胞迁移、增生及存活。体外及大鼠模型中,用一种靶向性针对多重酪氨酸激酶抑制剂的 BCR- 抗体 1、即达沙替尼,以及针对酪氨酸激酶 Src 家族的抑制性试验结果喜人。II 期试验阴性,但针对 DDR2 抑制的进一步研究仍在继续。
NSCLC 中的血管生成抑制
阻断肿瘤血供及血管生成,已经成为诱人多年的目标,且在部分其他恶性肿瘤如结直肠癌、卵巢癌和宫颈癌中已经取得了部分成功。据信有多种生长因子及细胞因子参与了血管生成中的复杂信号通路。其中关键性的两个生长因子为血管内皮生长因子(VEGF)及血小板源性生长因子(PDGF)。
有两项关键性 III 期试验证实,NSCLC 中用抗 VEGF 单克隆抗体贝伐单抗联合标准的含铂二联化疗进行靶向性血管生成抑制是有效的。美国东部肿瘤协作组(ECOG)研究证实仅用化疗时总生存中位数为 10.3 个月,而化疗加用贝伐单抗时为 12.3 个月。AvAil 试验表明,虽然总生存未见改善,但总有效率改善、无进展生存更长。
贝伐单抗的主要不良反应有出血、血栓栓塞、高血压。严重出血及咯血与组织学为鳞状细胞癌、具有侵蚀现象有关,因此以前的 II 期试验发现有致死性肺出血后,就限制了其临床仅能应用于非鳞的非小细胞肺癌。进一步在非鳞的 NSCLC 进行的 III 期试验(AVAPERL)表明,培美曲赛维持治疗加用贝伐单抗可能会有所改善。
小分子酪氨酸激酶抑制剂也可用于抑制 VEGF 通路。迄今为止,已有数种多重酪氨酸激酶抑制剂的 III 期试验未能表现出生存方面的临床获益。尼达尼布(nintedanib)联合二线化疗在无进展生存方面具有极为轻微的获益、但总生存无获益,预计亚组分析将表明组织学为腺癌的患者获益最多。
一种新型的抗血管生成药称之为肿瘤血管阻断剂,在临床前试验中并未见效果。III 期试验中 vadimezan 也未见获益,已经不再进行进一步研究了。对于抗血管生成治疗来说,未来应该是进一步研究以寻找恰当的预测性生物学标记。
总结
最近十年内,分子病理学的巨大进步已经使我们对 NSCLC 潜在病理机制及显著异质性的理解有了很大进展。目前也确定了多条信号通路及导致恶性转化的致癌性驱动突变。具体到临床实践,对肿瘤组织进行这类驱动突变的分子检测已经成为了常规。
目前而言,大部分肿瘤中仍未检测到驱动突变,因此对这类患者仍为细胞毒性化疗经验性治疗。对于具有已知驱动性突变的非小细胞肺癌患者,已经表现出了显著临床获益,但获得性耐药仍常见,且为我们制定独特的个体化治疗提出了下一个挑战。
既往经验有助于我们在靶向治疗道路上的探索。比如,克唑替尼用于 ALK 阳性患者,从开始 I 期试验、到 III 期试验得到阳性结果仅用了 6 年;仅 II 期试验的数据就得到了 FDA 的批准,此时仅仅四年。
未来,诊断治疗学的成功、真正肿瘤个体化治疗的关键,将是充分利用有限资源、通过预测性生物标志物确保筛选出恰当的患者并使得不良作用最低。至于耐药性方面,恰当应用抑制剂、或联合应用抑制剂,同时控制不良作用最低,有望在将来实现患者生存改善。
再进一步,真正的挑战将是把这些制剂运用到早期患者的治疗,以真正改善这种恶性病魔的治愈率。

-
奇葩老爸1 楼 2017-04-17 05:37:20
我老爸已经完成了第一阶段的化疗,持续了一年时间,开始产生耐药性,基因检测EGFR外显子20基因突变,属于何种靶向药比较有效果?
-
dfsy2 楼 2017-03-28 11:15:20
帖子好!
-
爱相随3 楼 2017-03-22 06:54:11
我想知道基因全阴,肺鳞吃什么药?
-
康康4 楼 2017-03-18 08:28:16
肺鳞癌
-
祈福祈喜5 楼 2017-03-05 02:12:08
详解技术的好帖!
-
荣知新6 楼 2017-02-04 09:59:26
感谢分享!
-
Toys & Costume8 楼 2017-01-29 12:31:13
靶向药物研究已经遇到瓶颈,第四代靶向药必须与化疗药同时使用才能发挥作用。最终出路是在于免疫治疗
-
bn9 楼 2017-01-15 09:35:38
看不懂啊,太专业了
-
妈妈10 楼 2017-01-15 12:51:41
好专业,有点看不懂

曾任美国临床肿瘤学会(ASCO)临床实践指南委员会主席
约翰霍普金斯医学院,医学博士
Lifespan癌症研究所胸部肿瘤科主任
曾在纽约纪念斯隆凯特琳癌症中心任职10年
曾在波士顿的麻省总医院癌症中心任职6年

 400-107-6696
400-107-6696



 肺癌帮
肺癌帮
 17465
17465
 15
15





 15858
15858






 京公网安备 11010502037180号
京公网安备 11010502037180号
 400-107-6696
400-107-6696


