都是EGFR基因突变,用药可能不一样!
 16866
16866
近年来,靶向治疗正不断朝着“更精准”的方向发展:即便是同一个基因突变,但突变亚型不同,靶向药的选择可能完全不一样。以晚期非小细胞肺癌常见的EGFR基因突变为例,主要包括Del19(19号外显子缺失)、L858R(21号外显子)以及T790M这几种突变亚型[1]。其中,Del19和L858R对一、二、三代靶向药都敏感;而T790M突变作为一种耐药突变,目前只能选择三代靶向药。
但最近有证据显示,虽然Del19和L858R都是EGFR突变,但靶向药对这两个突变亚型的疗效有着明显的差异。在接受相同靶向药治疗的前提下,L858R患者的疗效有限、生存期更短,而Del19患者的疾病进展风险则可下降25%-40%[2],且无进展生存期(PFS)和总生存期(OS)更长[2,3]。因此,有不少专家认为:Del19突变和L858R突变是两种不同的疾病,未来精准治疗可能可以做得更精准,对这两类突变患者区别治疗[4][5]。
比如,国外Bryan教授团队就开展了一项综合分析,汇总晚期非小细胞肺癌患者靶向治疗的选择,分析认为对于Del19患者,更合适的一线治疗方案似乎是直接使用二代靶向药阿法替尼[6]。而针对L858R突变,目前有部分临床学者认为,贝伐珠单抗联合厄洛替尼(即A+T)的治疗方案可能会帮助患者获得更长的PFS[7]。
Del19突变:一线治疗直接使用阿法替尼可能更合适
在临床治疗追求“精准再精准”的今天,无论从靶向药的有效性、安全性,还是成本效益来看,二代药阿法替尼可能更适用于Del19患者的一线治疗。
日本有一项临床前试验(pre-trial),把多个靶向药放在体外培养皿中测试它们对EGFR不同突变亚型的抑制能力[8]。研究发现,大多一代、二代和三代靶向药都有抑制Del19突变的能力,但二代靶向药阿法替尼的抑制能力尤为突出,在同等抑制癌细胞水平的前提下,阿法替尼所需的药物浓度更低,说明具有更强大抑制癌细胞的活性,而且阿法替尼的抑制范围几乎覆盖了所有的Del19突变(如delE746_A750、delE746_S752insV等更细分的亚型)。综合这两点来看,理论上阿法替尼可能更有效抑制Del19突变的癌细胞生长。

* IC50(半数抑制浓度)是临床前试验中评估药物抑制能力强弱的指标,该指标数值越小,说明药物的抑制能力越强。
从临床前研究了解靶向药抑制突变的能力只是第一步,药物在多中心、双盲等科学条件下设置的临床试验(clinical trial)中“脱颖而出”,才能更客观公正地反映出其疗效。在这方面,虽然阿法替尼没有和一代靶向药直接头对头地比较总生存期(OS),但对照之前一代药和化疗药一线治疗的临床研究,可以发现:

在Del19亚组人群的分析图中,数据点偏左代表阿法替尼在Del19患者群体中占治疗优势,偏右代表使用化疗更好,居中则代表二者没有明显的治疗优势差异。从数据点分布可知,阿法替尼对Del19突变更有“治疗倾向性”,而且在Del19患者中观察到显著的生存获益(OS)[9]。
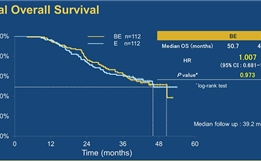
即便在真实世界中,患者实际获益与临床实验的对照结果也是一致的。在同为东亚人种的韩国,阿法替尼一线治疗Del19患者的中位PFS为19.1个月,远优于一代靶向药[11]。而在加拿大,由华裔Lau教授牵头的真实世界研究(Real World Study)发现,一线用阿法替尼和一代药治疗的Del19患者,OS分别是48.8月和26.4月,时长区别很明显[12]。


除了一线治疗的生存期长短,耐药后所能接受的二线治疗也是患者在选择用药时经常考虑的问题。研究发现,相较于一代靶向药,Del19患者一线使用阿法替尼,后续的获益可能会更好。首先,无论是一线使用一代靶向药或阿法替尼,Del19患者出现T790M耐药突变的概率都比较高。AURA2和AURA扩展研究合并分析证实[13],Del19患者一线治疗后出现T790M突变的比例达73%,说明约有3/4的Del19患者可以在二线治疗阶段用上第三代靶向药继续延长生命;其次,Del19患者序贯第三代靶向药治疗后的生存期也很可观。在一项名为GioTag的真实世界研究中[14],Del19患者首先使用阿法替尼,在出现T790M突变后序贯第三代靶向药治疗,前后两段治疗时长加在一起,中位治疗持续时间为30.6个月,中位OS长达45.7个月。换言之,Del19患者一线使用阿法替尼,最长可以获得近4年的生存期!


对于阿法替尼,大多患者的初印象是“副作用”。其实,一代、二代和三代靶向药都有不同程度的副作用。作为二代靶向药,阿法替尼除了对EGFR和HER2等基因突变进行广泛抑制(这意味着抑制癌细胞的效果更强),对于EGFR野生型也有一定的抑制作用,所以不可避免产生相关副作用,如皮疹、腹泻、甲沟炎、口腔溃疡等。但《EGFR-TKI不良反应管理专家共识》指出[15],类似的副作用大多可管理、可控制,只要及时采取预防和对症措施,都能最大程度帮助提升患者的生活质量。
与之相对的,患者可能更需要担心靶向药对身体造成的肝损伤。资料显示,大多EGFR靶向药都是通过肝脏酶代谢,这就容易导致患者肝损伤风险增高。尤其我国作为肝病大国,国人的肝毒性发生率相比全球就更高,在治疗肺癌的同时,如果伴有肝功能不良,服用靶向药将加剧肝损伤,有可能进而导致急性肝衰竭或亚急性肝衰竭,给生命带来危险。而阿法替尼是不经过肝脏代谢的靶向药,说明药物对肝功能的影响较小、更显著降低肝损伤风险。而且,对于轻中度肝功能损伤患者,阿法替尼不必调整起始剂量,所以从长期用药的角度考虑,阿法替尼可能更适用于存在轻中度肝功能不全的患者。
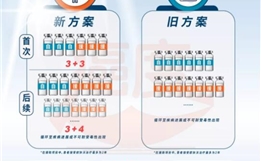
在成本效益方面,一线使用阿法替尼治疗晚期非小细胞肺癌已纳入医保,在序贯三代靶向药的前提下,预估总的治疗时间可达到29.7个月,花费约为23.6万[16]。相较于一线使用三代靶向药序贯化疗的治疗方案,足足节省了10万(以上价格为药物治疗费,患者实际支付的费用按各地医保自付比例计算),大大减轻了患者的经济负担。
L858R突变:A+T治疗方案获更长PFS
与Del19突变相比,L858R突变的生物学机制迥然不同,这可能是单用靶向药治疗获益不佳的原因之一。不过,科学家并没有“放弃”这一群体,一直在探索着新的治疗方案:近年研究发现,L858R突变的生物学机制使得其肿瘤具有更强的侵袭性,而侵袭强度可能与肿瘤新生血管相关。
基于上述观察,我国开展了一项ARTEMIS(CTONG 1509)的研究。研究发现,一代靶向药A(厄洛替尼)+抗血管生成药T(贝伐利珠单抗)的联合用药给L858R患者带来了更长的PFS获益[7]。研究纳入了311名来自中国的L858R患者,分成A+T联合治疗组和厄洛替尼单药组。其中,A+T联合治疗组的L858R患者,中位PFS达到19.5个月、降低疾病进展风险45%,而厄洛替尼单药组仅有9.7个月。与单药组治疗相比,A+T联合治疗组患者的PFS显著延长,因此A+T的治疗方案可能是L858R患者一线治疗的新选择。

随着临床对靶点生物学机制的理解越来越深刻和透彻,进一步挖掘药物在不同突变亚型的临床疗效,力求“更精准”的治疗,已经是当前靶向治疗的新趋势。期待在不远的将来,科学家能够借助更多的科研资源,在“精准靶向治疗”的道路上走得更远,通过不断推陈出新的临床数据,找到更优的治疗方案,为患者生命“续航”!
参考资料(可上下滑动查看) [1] Hengrui Liang, Zhenkui Pan, Wei Wang, et al. The alteration of T790M between 19 del and L858R in NSCLC in the course of EGFR-TKIs therapy: a literature-based pooled analysis. J Thorac Dis. 2018 Apr; 10(4): 2311–2320.
[2] Yaxiong Zhang, Jin Sheng, Shiyang Kang, et al. Patients with Exon 19 Deletion Were Associated with Longer Progression-Free Survival Compared to Those with L858R Mutation after First-Line EGFR-TKIs for Advanced Non-Small Cell Lung Cancer: A Meta-Analysis. PLoS One. 2014; 9(9):e107161.
[3] Lee CK, Wu YL, Ding PN, et al. Impact of specific epidermal growth factor receptor (EGFR) mutations and clinical characteristics on outcomes after treatment with EGFR tyrosine kinase inhibitors versus chemotherapy in EGFR-mutant lung cancer: A Meta-analysis . J Clin Oncol. 2015;33:1958–1965.
[4] 肿瘤资讯. 吴一龙教授:EGFR 19del突变和21L858R突变晚期NSCLC的一线治疗或需分别考虑
[5] 肿瘤资讯. 褚倩教授:EGFR 19del和21L858R突变阳性NSCLC的差异与治疗选择
[6] Bryan Oronsky, Neoplasia. 20 (1), 92-98 Jan 2018
[7] Zhou Q, Wu Y L, Cheng Y, et al. CTONG 1509: Phase III study of bevacizumab with or without erlotinib in untreated Chinese patients with advanced EGFR-mutated NSCLC [J]. Annals of Oncology, 2019, 30(v603.
[8] Kobayashi Y, et al. Cancer Sci. 2016;107(9):1179-1186.
[9] Kato T et al., ISPOR 2015; PCN40
[10] Tu et al. Oncotarget.2018 Feb 4;9(36):24237-24247.
[11] Youjin Kim. Cancer Res Treat. 2019 Aor;51(2):502-509.
[12] Lau SC et al. Clin Lung Cancer. 2019 May 11. pii: S1525-7304(19)30107-X
[13] Jenkins S et al. J Thorac Oncol. 2017 Aug;12(8):1247-1256.
[14] Hochmair MJ et al. Future Oncol. 2019 Sep;15(25):2905-2914.
[15] EGFR-TKI不良反应管理专家共识,中国肺癌杂志2019年2月第22卷第2期 Chin J Lung Cancer, February 2019, Vol.22, No.2
[16] 颜建周,等. 一线使用阿法替尼与一线使用奥希替尼治疗表皮生长因子受体常见突变非小细胞肺癌的预算影响. 中国药物经济学. 2020, 15(6): 5-17.

 400-107-6696
400-107-6696






 34845
34845
 0
0






 京公网安备 11010502037180号
京公网安备 11010502037180号
 400-107-6696
400-107-6696


