EGFRm早期NSCLC患者辅助靶向治疗迎来新曙光
 16495
16495
【疾病背景概览】
肺癌是目前全球肿瘤发病率及死亡率第一的肿瘤,每年导致超过170万例患者死亡。其中非小细胞肺癌(NSCLC)占所有肺癌病例的85%,约1/3患者在诊断时可行手术治疗。手术作为早期NSCLC的主要方式,是目前唯一可以治愈肺癌的手段,但是除IA期患者外,IB-III期的治愈率并不乐观,IB/II/IIIA期的5年复发率分别是45%, 62%, 76%,依然有非常多的患者在手术后会发生复发,继而进展为晚期肺癌。
【辅助化疗历程回顾】
回顾辅助治疗的探索历程,迄今为止,化疗仍是完全切除术后NSCLC唯一延长生存的治疗方式。IALT、JBR.10和ANITA三个大型随机研究提示辅助化疗取得阳性结果, LACE荟萃分析共纳入了5项大型临床研究,4584例患者随访5.2年的结果提示早期NSCLC患者接受辅助化疗可获5年OS获益,5年生存率增加5.4%,死亡风险显著下降11%(HR=0.89,P=0.005)。基于以上研究的数据,NCCN指南、CSCO等国内外各大指南已经将术后辅助含铂方案化疗作为II期和III期NSCLC可手术患者的标准治疗推荐。尽管术后辅助化疗确实对OS有所改善,但通过分析可以看到辅助化疗延长5年生存率的患者比例非常有限,同时化疗较严重的毒副作用也导致相当一部分患者因无法耐受,而无法完成整个化疗方案。
【辅助靶向早期探索】
众所周知,在晚期NSCLC的治疗探索中,2009年IPASS研究开启了肺癌精准治疗时代,自此肺癌的靶向治疗便进入了复杂而精细的治疗阶段。早期肺癌的辅助靶向治疗尽管从2002年的BR.19研究便开始探索,但由于早年治疗对于精准治疗的认知有限,所以前期进行的辅助靶向治疗都未取得成功。BR19研究未对研究人群进行选择,RADIANT研究则选择的并不是EGFR突变的患者,而是EGFR免疫组化和/或FISH阳性的患者。所以这两个研究不管是其主要研究终点DFS,还是OS都未做出阳性结果。但RADIANT研究EGFR突变阳性亚组的分析依然给了一些启示,TKI组的DFS有获益趋势。之后进行的SELECT单臂II期研究也证实了其2年的DFS率要优于历史数据,这些早期对辅助靶向治疗的探索虽然存在各自的局限性,但却给我们带来了诸多思考,包括研究对象需要精准的针对合适人群,与辅助化疗如何组合,纳入患者分期的选择等。这些早期的研究也给辅助靶向治疗的进展带来了一线曙光。
【辅助靶向治疗研究进展】
ADJUVANT研究(CTONG1104)
ADJUVANT研究是首个在EGFRm人群头对头比较TKI和化疗辅助治疗疗效的III期随机对照研究,是具有一定开创性的大型研究。这项研究是针对的II-IIIA(N1-N2)的NSCLC患者,给予两年的吉非替尼辅助治疗与长春瑞滨联合顺铂(VP)辅助治疗进行头对头比较的随机对照研究,主要终点指标DFS取得了显著延长,辅助靶向30.8个月对比辅助化疗19.8个月,HR=0.56,p值为0.001。今年ASCO会议更新了其OS数据,辅助靶向75.5个月对比辅助化疗的62.8个月,HR=0.92,p值为0.067,遗憾的是,前期取得的DFS显著获益并未转变成最终的OS获益。虽然OS没有取得显著性统计学差异,但确实有约13个月生存获益的延长,与历史数据相比,吉非替尼辅助治疗组的OS是完全切除的IIB-IIIA NSCLC最好的OS之一。这一研究结果提示R0切除N1-N2期EGFR突变阳性的NSCLC患者进行2年的TKI辅助治疗是可行的,给这部分患者带来了更多的治疗选择。
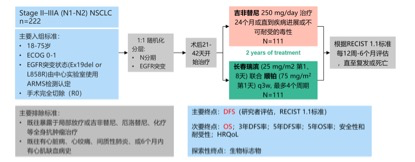
ADJUVANT研究设计
ADJUVANT研究主要终点DFS
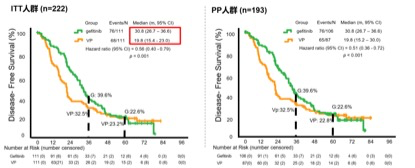
ADJUVANT研究次要终点OS

ADAURA研究
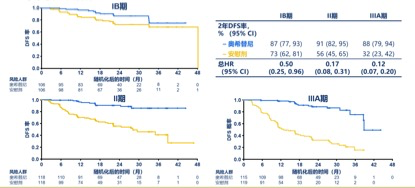
今年ASCO会议ADAURA研究数据的提前揭盲,揭示了三代TKI在辅助治疗领域的未来获益趋势,结束了之前较为漫长的等待。ADAURA研究是一项全球性的III期双盲随机研究,评估在完全切除的IB-IIIA非鳞状细胞EGFR突变阳性NSCLC患者中,奥希替尼与安慰剂对比的有效性和安全性,其计划内的主要终点分析原定是在2022年揭晓,但由于IDMC(独立数据监测委员会) 安全性评估中观察到奥希替尼在EGFR突变阳性非小细胞肺癌辅助治疗中取得压倒性疗效,出于伦理考虑,建议提前揭盲。ADAURA研究在设计上与ADJUVANT研究最大的区别是,ADAURA研究并不是要用辅助TKI替代化疗,而是在辅助化疗之后用靶向治疗和安慰剂做比较;ADAURA研究中辅助靶向使用的时间是三年而非两年。主要研究终点II-IIIA期患者的DFS HR 达到 0.17,是目前已知最好的HR值;次要研究终点IB-IIIA期患者的DFS HR 达到 0.21,提示全人群获益,奥希替尼组在IB,II和IIIA期中的2年DFS率差别不大,分别是87%,91%和88%,侧面说明在数据报道时,不同分期奥希替尼组的患者疾病仍在控制中,而对照组已经出现了复发。另外,奥希替尼安全性的分析也与已知的奥希替尼安全性一致,可长期耐受。
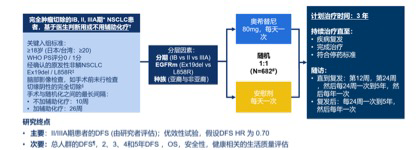
ADAURA III期双盲研究设计
ADAURA研究主要终点
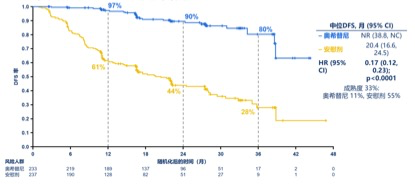
不同分期的DFS
现阶段我们的临床实践可能面临的已经不再是做不做辅助靶向治疗,而是如何更好做辅助靶向治疗,因此就需要我们就以下问题进行探讨。
1) 是否需要等待OS最终结果再修改临床指南?
部分临床专家认为需要OS结果再改变临床实践,DFS不能完全替代OS;而另一部分临床专家则认为基于ADAURA研究的HR值,以及DFS与OS之间的关联性,替代研究终点DFS已足够。回答这个问题之前需要我们先解答:对于可手术患者是不是可看待为可治愈性疾病?如果是,那么单纯的DFS延长肯定是不能满足临床需求的,总生存的延长才是硬道理;如果否,那DFS的意义将极为重大,特别对于IIIA期患者,2年的复发率高达78%。目前II -IIIA期可手术患者的复发率提示只有小部分患者可治愈,大部分仍为不可治愈疾病,所以DFS可能就足以判断对于这些患者的获益。
2) 是否要先进行辅助化疗再进行辅助靶向治疗?
ADJUVANT研究给我们的提示是无需进行辅助化疗,同样可以取得比辅助化疗更好的DFS和无差别的OS;而ADAURA研究也间接说明了这个问题,即无论患者是否既往接受过辅助化疗,都有一致的DFS获益,HR值都在0.2左右,所以对于是否进行辅助化疗还是根据临床医生既往的经验进行判断。
还需要考虑的是辅助治疗的目的是清除术后的微小残留灶,尽可能减少疾病复发率。如果辅助靶向单药就能清除掉所有的微小残留灶,或者大幅清除到一定程度,同时依靠免疫系统维持长期的清除平衡,那么辅助TKI单药即可满足临床需求。如果不足以控制微小残留灶在非常小的程度,也仅仅只是推迟复发时间,那么其实还是有必要考虑先进行辅助化疗的。另外,由于辅助治疗还需要考虑安全性的问题,尤其是药物相关的死亡,因此应该优选疗效更好且毒副作用更低的治疗方案。
【辅助靶向治疗未来需要解决的问题】
1.辅助靶向治疗人群:IB,II,IIIA?
当前,辅助治疗主要是推荐NSCLC高复发风险患者(II-IIIA期),在高危IB期NSCLC患者中也可以考虑使用辅助治疗。在II-IIIA期EGFRm NSCLC患者中,特别是在高复发风险的患者中,与化疗相比,辅助EGFR-TKI治疗可使患者获得更长的DFS。但IB期患者能否从辅助治疗中获益及是否涉及过度治疗,目前仍存在争议,可能还需要进一步研究把IB期中高危人群筛选出来。所以,EGFR-TKIs确实给患者提供了一种新的辅助治疗选择,但是治疗的选择依然应取决于临床医师对患者临床获益和风险的评估。
2.辅助靶向治疗模式:
ADD模式(辅助化疗+辅助靶向) vs OR模式(辅助靶向)OR模式主要来自ADJUVANT研究设计,此项研究是头对头比较辅助TKI 和辅助化疗的疗效;而ADD模式则是参考ADAURA研究在化疗基础上应用辅助TKI治疗,所以究竟哪个是更好的治疗模式也是目前临床专家比较困惑的地方。ADAURA研究中辅助化疗后接受奥希替尼治疗的患者(55%)和未接受辅助化疗即开始奥希替尼治疗的患者(45%)的结果均显示奥希替尼有效。但考虑到ADD模式可以最大限度清除术后的微小残留灶,尽可能减少疾病复发率,因此在安全可控的情况下,可以首选辅助化疗联合靶向治疗的ADD模式。
3.辅助靶向治疗时间:
2年 vs 3年?既往EGFR-TKIs辅助治疗临床试验通常设置为2年的治疗期(如SELECT, RADIANT, ADJUVANT),但研究发现一代TKI辅助治疗最高的复发率往往出现在停药后的12个月内。而在其它肿瘤(如ER+或Her2+乳腺癌)的辅助靶向药物治疗中,现有研究提示靶向药物持续时间越长,疗效越好。比如伊马替尼辅助治疗胃肠间质瘤(GIST)时间,目前的研究结果提示5年对比3年治疗存在一定的潜在优势,提示辅助靶向治疗用药越长越好。加之奥希替尼具有良好的安全性,在辅助治疗中较长时间的持续治疗可能比其他EGFR-TKIs更可行,所以ADAURA研究进一步探索了EGFR-TKI辅助治疗3年的生存获益。从科学角度,现有数据可能支持更长的用药时间;而从社会层面考虑,政府机构可能会考虑药效经济学和疗效获益性价比的问题,这中间的平衡还需要政府、医生、患者及企业多方协调才能将三代TKI在早期肺癌中的科学价值在临床实践中得以实现。
4.辅助靶向治疗后进展模式:
ADJUVANT研究报道了早期肺癌术后辅助靶向治疗复发模式的探索,首次证实了吉非替尼和化疗治疗后的复发转移时空变化是完全不同的,并且吉非替尼辅助治疗对于控制术后复发转移的疗效要优于辅助化疗,尤其是控制颅外转移方面,无论是脑转移还是颅外转移,辅助吉非替尼治疗都显著推迟了复发风险的高峰时间。而众所周知,奥希替尼有更强的血脑屏障穿透能力,在FLAURA研究中提示能更加有效控制颅内复发,推迟颅内复发风险,因此可能会有不同的复发进展模式,也期待后续ADAURA研究数据更加成熟后,能尽快报道复发进展模式。
5.辅助靶向治疗进展后用药选择:
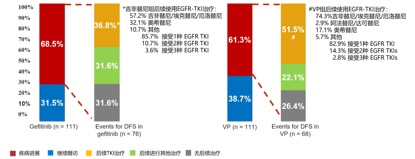
ADJUVANT研究的事后分析提示在辅助化疗组61.3%的复发患者中,仅有51.5%在后续又接受了辅助靶向治疗,也就是说仅有一半的患者在全病程治疗中能用上靶向治疗。考虑到ADJUVANT研究是在大型的研究中心开展的RCT研究尚且如此,那么真实世界中将有相当一部分患者在全程治疗中没有机会接受靶向治疗。在ADJUVANT的后续治疗OS分析中,生存最差的患者就是F组仅仅接受了化疗的患者,这些患者终身未接受靶向治疗,所以对于这部分患者可能有必要把靶向治疗进行前移,以确保更多患者能接受靶向治疗。
事后分析:疾病进展后的后续治疗方案分析
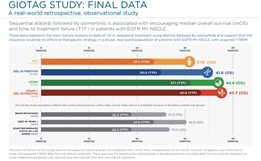
事后分析:不同治疗组合的OS

总结来说,我们看到ADAURA研究的提前揭盲给早期肺癌的辅助治疗上提供了更多选择,未来也有可能成为改变临床实践的重要研究,我们也期待更为成熟的数据解答临床上目前尚未解决的问题,给临床医生提供更多的证据基础。
参考文献:1. World Health Organization. Globocan Worldwide Fact Sheet 2018. Available at: http://globocan.iarc.fr/Pages/fact_sheets_population.aspx. Accessed May 14, 2020.2. Cancer. net. Available at: https://www.cancer.org/content/dam/cancer-org/cancer-control/en/cancer-types/non-small-cell-lung-cancer-complete.pdf Accessed May 14, 20202.3. Datta et al. Chest 2003;123: 2096–2103.4. Le Chevalier Ann Oncol. 2010;21 Suppl 7:vii196–8.5. Cagle et al. Arch Pathol Lab Med. 2013;137:1191–1198.6. AJCC Cancer Staging Manual. 7th edn. Springer, 2010. NSCLC,非小细胞肺癌.7. Chansky et al. J Thorac Oncol 2017;12:1109–1121.8. Kris et al. J Clin Oncol 2017;35:2960–2974.9. Pignon et al. J Clin Oncol 2008;26:3552–3559; 4. AJCC Cancer Staging Manual. 7th edn. Springer, 2010.10. Non-small cell lung cancer collaborative group, BMJ 1995; 311:899-909.11. PignonJP, et al. J Clin Oncol 2008;26:3552-9.12. Goss GD, et al. J Clin Oncol. 2013 Sep 20;31(27):3320-3326.13. Kelly K. J Clin Oncol. 2015.Dec 1;33(34):4007-4014.14. Yi-Long Wu, Lancet Oncol, November 21, 2017.15. 2020 ASCO Abstract 9005 by Yi-Long Wu. Roy Herbst, et al,. 2020 ASCO virtual meeting, LBA5

 400-107-6696
400-107-6696






 15837
15837
 0
0






 京公网安备 11010502037180号
京公网安备 11010502037180号
 400-107-6696
400-107-6696


